Die Geburt des Kollektivs
Wenn sich Bakterienzellen zu Matten zusammenlagern, könnte dies der erste Schritt auf dem Weg zu einem Organismus sein
Wer betrügt, kann gehen. Im Fall der Bakterien im Labor von Paul Rainey ist genau das sogar gewünscht. In seinem Labor am Max-Planck-Institut für Evolutionsbiologie in Plön untersucht der Evolutionsbiologe, wie aus einzelnen Zellen ein vielzelliger Organismus wird. Zu viel Zusammenhalt kann demnach kontraproduktiv sein.
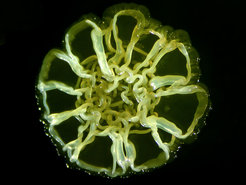
Überproduktion eines Cellulosepolymers
zur Folge haben. In flüssigem Nährmedium bilden die Bakterien eine dichte Matte.
Text: Magdalena Nauerth
Als das Leben entstand, gab es noch nicht viel Zusammenhalt. Die ersten Zellen waren «Einzelkämpfer», die sich an die rauen Lebensbedingungen auf der Erde vor 3,8 Milliarden Jahren anpassen mussten. Aber nur 300 Millionen Jahre später haben sich die ersten Bakterien zusammengetan. Das erste mehrzellige Leben auf der Erde ist in Westaustralien als sogenannte Stromatolithen erhalten geblieben. Die ersten Zellen mit einem Zellkern erschienen vor 2,7 Milliarden Jahren und mehrzelliges eukaryotisches Leben vor 1,7 Milliarden Jahren. Rainey und sein Team wollen verstehen, wie Einzelzellen den Übergang zu Vielzellern geschafft haben könnten.
Paul Rainey hat Biologie studiert. Nach dem Studium hatte der Neuseeländer von seinem Fach jedoch erst mal genug und tourte mit seinem Saxofon als Jazzmusiker mehrere Jahre durch die Welt. Nachdem er seit seiner Rückkehr nach Neuseeland zwischenzeitlich für ein Molkereiunternehmen als Verkaufsleiter gearbeitet hatte, besann er sich auf seine alte Leidenschaft, die Biologie, und schrieb sich wieder an der Universität ein. Für sein Masterprojekt sollte er Pilze untersuchen.
Schon damals wurde er auf ein Bakterium namens Pseudomonas tolaasii aufmerksam, das Pilze befällt. Es bewegt sich mithilfe seiner fadenförmigen Geißeln vorwärts. Rainey bemerkte, dass sich Pseudomonas an wechselnde Bedingungen in seinen Kulturgefäßen anpassen konnte. Manche dieser Zellen verloren die Fähigkeit ein Gift zu produzieren, das bei Pilzen Gewebeschäden auslöst. Das Bakterium hat ihn seitdem nicht mehr losgelassen. Neben seinen eigentlichen Forschungsprojekten hatte er immer auch Experimente mit Pseudomonas am Laufen.
Diese enorme wissenschaftliche Neugier gepaart mit Beharrlichkeit sollte sich letztlich auszahlen, sie brachte ihm aber auch manchmal gehörigen Ärger ein. Als Rainey nach seiner Doktorarbeit für ein weiteres Forschungsprojekt zu Pilzen nach Großbritannien wechselte, beobachtete er, dass die Bakterien in seinen Kulturen neben den typischen halbkugeligen, glatten Kolonien auch andere Formen hervorbrachten. Die Zelloberfläche des zweiten Typs war von tief eingeschnittenen Furchen übersät. Rainey nannte sie deshalb „schrumpelige Streuer (wrinkly spreaders)“. Diese Zellen bildeten auf der Oberfläche von flüssigen, ungeschüttelten Nährmedien eine dichte Matte. Der andere Typ besaß ein „flaumiges“ Aussehen, daher der Name „flaumige Streuer (fuzzy spreaders)“. Wie die Schrumpeligen bildeten auch sie aufgrund elektrostatischer Anziehung zwischen den Zellen Matten – in diesem Fall allerdings nur kurzlebige.
Sauerstoffmangel schafft Vielfalt
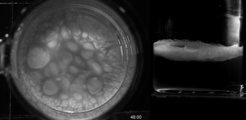
Cellulosepolymers haften die Zellen aneinander und am Rand des Kulturgefäßes. Dadurch bleiben
sie an der Grenzfläche von Luft und Flüssigkeit, wo sie mit reichlich Sauerstoff versorgt werden. (rechts im Bild die Seitenansicht.)
Raineys Tests ergaben, dass die Kolonien nicht nur verschieden aussahen, sondern auch aus Zellen mit unterschiedlichen Eigenschaften bestanden. War das schon Evolution? „Zu diesem Zeitpunkt verstand ich noch nicht die Bedeutung von dem, was ich da vor mir sah“, erzählt Rainey. Im weiteren Verlauf seiner Forschung zeigte sich, dass die Varianten immer nur dann auftraten, wenn die Kulturgefäße, in denen die Bakterien züchteten, ruhig standen und nicht geschüttelt wurden. Durch das Schütteln sollte die Versorgung mit Sauerstoff in der Nährlösung sichergestellt werden. In ungeschüttelten Gefäßen brauchten die Mikroben das lebenswichtige Gas dagegen schnell auf. In dieser Lage kamen die schrumpeligen und flaumigen Streuer ins Spiel: Dank der Fähigkeit von Zellen unterschiedlicher Kolonietypen zum Zusammenhalt konnten diese Matten bilden und den hohen Sauerstoffgehalt an der Oberfläche zu nutzen.
Immer wieder kam Rainey mit seinem Experiment zum gleichen Ergebnis: Nach ein paar Tagen entstand eine Mischung aus glatten, schrumpeligen und flaumigen Zellen. Sie erschienen sogar stets in der gleichen Reihenfolge: zuerst die runden, dann die schrumpeligen und zuletzt die flaumigen. „Das war der Durchbruch: Pseudomonas hatte sich also an Sauerstoffmangel angepasst“, sagt Rainey rückblickend.
So aufregend diese Ergebnisse auch waren, bei seinem damaligen Arbeitgeber kamen sie nicht so gut an, denn eigentlich sollte in eine andere Richtung forschen. Und so wurde ihm untersagt, seine Experimente fortzuführen. Aber Rainey machte trotzdem weiter – wenn auch auf eine diskretere Art und Weise. Zur Erforschung von Evolution sind die Pseudomonas-Bakterien ein ideales Modell. Anders als in freier Natur können die Forschenden im Labor die Lebensbedingungen ihrer Schützlinge genau kontrollieren. Und noch einen weiteren Vorteil hat die Arbeit mit Bakterien: Da die Evolution meist sehr langsam arbeitet, lässt sich bei den meisten Populationen nur über viele Jahre hinweg beobachten, welche Änderungen im Erbgut das Überleben beeinflussen. Anders bei Pseudomonas: Zwischen den Generationen liegt weniger als eine Stunde, evolutionäre Anpassungen lassen sich da wie im Zeitraffer studieren. „Wir konnten Evolution also im Reagenzglas untersuchen.“
Evolution im Labor

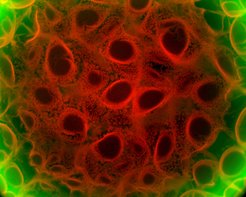
fluorescens seinen Namen gibt. In den Reagenzgläsern schwimmen die Mikroben in
verschiedenen Stadien ihres Lebenszyklus.
Seine Experimente haben Rainey zu einem der Mitbegründer einer neuen Teildisziplin der Evolutionsbiologie gemacht: der experimentellen Evolution. Inzwischen erforschen Wissenschaftler und Wissenschaftlerinnen rund um die Welt mit Experimenten, wie sich Organismen an Veränderungen der Lebensbedingungen anpassen. In den künstlichen Laborumgebungen, in denen die Forschenden jeden Parameter unter Kontrolle haben, geht das besonders gut. So ist Darwins ursprüngliche Evolutionstheorie durch natürliche Auslese heute vielfach wissenschaftlich belegt.
Aber wie wurden nun die einzelgängerischen Bakterien zu Teamplayern? Zunächst mussten sie überhaupt einmal zusammenbleiben können. Genetische Analysen von Rainey und seinem Team ergaben, dass die Matten-bildenden Zellen dank Mutation ein klebriges Zellulose-artiges Polymer produzierten. „Dieses Molekül wirkt wie ein Kleber, durch den sich die Bakterien an die Gefäßwand und aneinander heften können“, erklärt Rainey. So können sie an der Oberfläche einer Flüssigkeit eine Matte bilden und dort den höheren Sauerstoffgehalt nutzen. Für die Gemeinschaft ist dies eindeutig ein großer Vorteil. Aber für die einzelnen Zellen? Sie müssen ja für die Energie für das Kleberpolymer aufkommen. Pseudomonas erfüllte damit die klassische Definition von Kooperation: ein Verhalten, mit dem ein Individuum etwas zum Nutzen anderer beisteuert – auf Kosten des eigenen Vorteils. „Wir haben damit zum ersten Mal beobachtet, wie kooperatives Verhalten von Grund auf neu entstanden ist“, erzählt Rainey.
Zusammenarbeit ist in vielen Sozialverbänden im Tierreich zu finden. Bei den Bienen zum Beispiel kümmern sich Arbeiterinnen um die Aufzucht ihrer Schwestern, ohne sich selbst fortzupflanzen. Da sie sich aber genetisch sehr ähnlich sind, tragen sie so trotzdem zur Weitergabe ihrer Gene bei. Das Bienenvolk kann dadurch neue Bienen hervorbringen. Damit sich das Verhalten aber durchsetzen kann, müssen sich auch die Völker selbst vermehren. Sie tun das, indem eine junge Königin im Frühling mit einem Teil des Volkes den alten Stock verlässt und ein neues Bienenvolk gründet. Und die Bakterienmatten, können sie Baby-Matten produzieren? „Auf den ersten Blick schienen sie sich nicht fortpflanzen“, erzählt Rainey. Ohne Fortpflanzung ist jedoch keine Selektion möglich, denn die Selektion setzt nicht an den Matten an. Mit anderen Worten: Während Matten-bildende Zellen sich vermehren, sind die Matten selbst evolutionäre Sackgassen.
Leben auf Kosten der anderen
Paul Rainey und sein Team gaben aber nicht auf und beobachteten ihr evolutionäres Testsystem weiter. Mit der Zeit entstanden in den Matten weitere Typen mutierter Zellen, die den Klebstoff nicht mehr produzierten und sich frei bewegen konnten. Sie profitierten also vom Zusammenhalt des Verbandes und einer Versorgung mit Sauerstoff, ohne selbst dazu etwas beizutragen. „Sie betrügen ihre Kollegen in gewisser Weise. Da sie sich so die Produktion des Klebers sparen, können sie sich schneller vermehren. Gleichzeitig schwächen sie den Zusammenhalt der Matte und führen mit der Zeit deren Auflösung herbei“, so Rainey.
Die vorherrschende Meinung unter Forschenden lautet, dass solche Trittbrettfahrer ein Problem sind, das gelöst oder minimiert werden muss, weil Individuen sonst nicht dauerhaft zusammenarbeiten. Rainey und Kollegen stellten jedoch fest, dass die Betrüger eine ganz wichtige evolutionäre Funktion besitzen können: Unter bestimmten Bedingungen können sie dem Zellkollektiv bei der Vermehrung helfen. „In gewisser Weise nehmen die Betrüger die Rolle von Fortpflanzungszellen einnehmen, mit denen sich vielzellige Organismen vermehren. Die kooperierenden Zellen der Matte wären dann die Körperzellen. Mit dieser Trennung zwischen im Verband bleibender und sich verbreitender Zellen besitzen die Bakterienmatten schon ein Merkmal eines mehrzelligen Organismus“, erklärt Rainey.
Spezielle Zellen für die Ausbreitung
Anders als in den Reagenzgläsern der Forschenden können sich die Bakterienmatten in der Natur ausbreiten – zum Beispiel, indem sie sich in einem Weiher an die Schilfohre anheften. Wenn Schilfrohre frei werden, weil Matten sich ablösen und zu Boden sinken, können sich die frei beweglichen Verbreitungszellen anderer Matten die neue Nische besiedeln. Nun konkurrieren nicht mehr einzelne Zellen um Platz und Ressourcen, sondern die Matten. Diese werden nun Gegenstand der Selektion. Der am besten angepasste Verband verdrängt unterlegene Konkurrenten. „Dies bedeutet, dass die Selektion nicht mehr nur auf der Ebene einzelner Zellen ansetzt, sondern auf der der Matten“, sagt Rainey. „Eine solche Gruppen-basierte Selektion unterstützt die Entstehung komplexer Organismen“, erklärt Rainey. Die Ergebnisse brachten Rainey auf die Spur eines neuen Konzepts. Dieses berücksichtigt die zentrale Rolle der Ökologie bei großen evolutionären Übergängen wie beim Übergang von Materie zu den ersten selbstreplizierenden Molekülen, von Genen zu Chromosomen oder von Zellen zu mehrzelligen Organismen.
Meilensteine der Evolution
Evolutionäre Übergänge beginnen mit einfachen Einheiten, die sich zusammenschließen. Sie sind abgeschlossen, wenn das daraus hervorgehende Kollektiv an der Evolution durch natürliche Selektion teilnehmen kann. Dazu müssen die Gemeinschaften drei Eigenschaften besitzen: Sie müssen individuell verschieden sein und variieren, sie müssen sich fortpflanzen und ihre Eigenschaften an Nachkommen weitergeben. Den frühen Formen von Kollektiven fehlten diese Fähigkeiten jedoch. Folglich konnten sie nicht auf Basis natürlicher Selektion entstanden sein. Wie erklärt sich dann aber den Ursprung dieser grundlegenden darwinistischen Eigenschaften von Variation, Replikation und Vererbung?
Zusammen mit seinen Kollegen Andrew Black und Pierrick Bourrat hat Rainey ein Modell entwickelt, das die experimentellen Ergebnisse seines Teams vereinfacht und verallgemeinert. Es zeigt, wie ökologische Bedingungen dazu führen können, dass Kollektive die darwinistischen Eigenschaften Variation, Replikation und Vererbung ausbilden. Auf die Bakterienmatten im Teich bezogen bedeutet das: Die räumlich voneinander getrennt wachsenden Schilfstängel, an denen sich die Matten ansiedeln, ermöglichen Variation zwischen den Matten. Wenn Matten ausfallen, können neu verfügbare Schilfrohre durch Ausbreitungszellen besiedelt werden. Die Verbreitung und Wiederherstellung einer neuen Matte ist vergleichbar mit der Fortpflanzung der Matten. Und wenn das neue Kollektiv aus einer einzigen Zelle einer elterlichen Matte gebildet wird, dann erbt die neu gebildete Gemeinschaft die Eigenschaften der Eltern. «Die Matten selbst würden gar nicht als evolutionäre Einheiten an der natürlichen Selektion teilnehmen», erklärt Rainey. „Aber die ökologischen Bedingungen bewirken, dass sich ein darwinistischer Prozess auf der Ebene der Matten entfaltet.“ Allerdings müssen diese von außen auferlegten Eigenschaften zu inhärenten Merkmalen der neuen Lebensform werden.
Anhand von Experimenten und Computermodellen haben Rainey und seine Kollegen gezeigt, dass dies möglich ist. So haben Rainey und sein Team am Max-Planck-Institut beobachtet, dass die Bakterienzellen einen einfachen genetischen Schalter entwickeln, der den Übergang zwischen klebrigen Matten- und nicht-klebrigen Vermehrungszellen ermöglicht. Sie sind also nicht mehr auf zufällige Mutationen angewiesen, sondern besitzen getrennte Lebenszyklen für Wachstum und Vermehrung. In der Natur könnten die Matten schließlich die Fähigkeit erlangen, auf der Wasseroberfläche zu schwimmen. Dies würde sie unabhängiger von ansonsten einschränkenden Umweltbedingungen machen. Damit würde die Bakterienmatte vielzelligen Lebensformen ähneln, die ihre Fortpflanzungszellen ins Wasser abgeben.
Mit dem Konzept einer Kontinuität zwischen Organismus und Umwelt haben die Forscher dazu beigetragen, die Aufmerksamkeit auf die Bedeutung der Ökologie und von Umgebungen zu lenken, in denen darwinistische Eigenschaften auf neu entstandene Kollektive übertragen werden können. Dies öffnet die Tür zu neuen Experimente, mit denen Forschende die großen evolutionären Übergänge erklären können, einschließlich des größten von allen: der Entstehung des Lebens selbst.
Ob die ersten Zellen tatsächlich genauso wie in Raineys Experimenten zusammengefunden haben, ist unklar. An zu viele Veränderungen musste sich das Leben seitdem anpassen. Hinzu kommt, dass es viele verschiedene Wege zur Vielzelligkeit gegeben hat – je nachdem, in welcher Umwelt sich ein Organismus entwickelt hat. Im Laufe der Evolution ist Vielzelligkeit also mehrfach unabhängig voneinander entstanden. «Es ist aber durchaus plausibel, dass einer der Wege dem in unseren Experimenten ähnelt», sagt Rainey.
Auf den Punkt gebracht:
- Durch ihre kurze Generationszeit können sich Bakterien schnell an neue Lebensbedingungen anpassen. An Bakterienkulturen lässt sich Evolution deshalb im Labor wie im Zeitraffer beobachten.
- Wenn der Sauerstoff in Nährlösungen knapp wird, produzieren einzelne Bakterienzellen ein klebriges Polymermolekül, mit dem sie schwimmende Zellmatten bilden können. Auf diese Weise können sie den höheren Sauerstoffgehalt an der Oberfläche nutzen.
- Manche Zellen sparen sich die Kosten des Gemeinschaftslebens. Sie schaden zwar kurzfristig dem Bestand der Matten, können aber für die Vermehrung der Verbände genutzt werden. Nehmen die Trittbrettfahrer jedoch überhand, geht die Bakteriengemeinschaft zugrunde.
- Einfache ökologische Faktoren wie die ungleiche Verteilung von Ressourcen und die Fähigkeit zur Verbreitung ermöglichen die Evolution von Kollektiven.



